| 标识符 | CSTR:16397.09.0H16001256 |
|---|---|
| 资源中文名称 | AAV注射诱导恒河猴亨廷顿模型 |
| 资源英文名称 | Modeling Huntington's disease using intracerebral injections AAV overexpressing mutant HTT in rhesus monkey |
| 疾病概述 | 亨廷顿病(Huntington's disease, HD),又称大舞蹈病或亨廷顿舞蹈症(Huntington's chorea),是一种常染色体显性遗传性神经退行性疾病。 |
| 实验动物背景信息 | 选择雄性、年龄5-6周岁、体重5-7公斤的恒河猴。 |
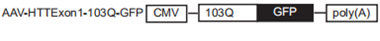
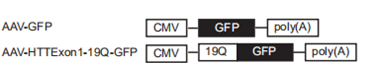
| 模型制作方法 | 1、实验材料 (1)实验动物:猕猴,5-6周岁,体重5-7公斤 (2)试剂:AAV-Exon1-103Q-GFP、三碘三酰苯、盐酸氯胺酮、异氟烷 (3)仪器:脑立体定位仪、X光机、微量注射泵、麻醉机 2、实验环境 普通级动物饲养设施,明暗交替时间:12/12,动物单笼饲养,笼具内有玩具等丰容措施。 3、腺相关病毒载体构建 AAV-Exon1-103Q-GFP:
对照采用AAV-GFP和1-19Q
|
| 模型表型数据 |
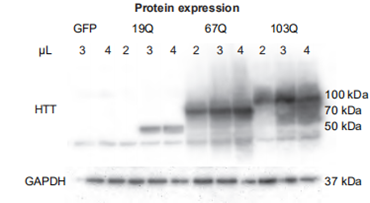
AAV转染后HTT表达明显增加(Fig 1)。
Fig 1. Confirmation of protein expression by western blot
与对照组相比,AAV注射组动物并未出现明显的解剖学异常等。
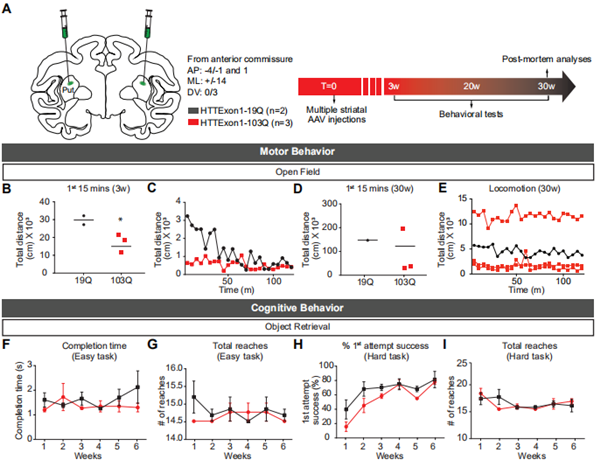
(1)Viewpoint视频监测系统检测动物运动量 在脑立体定位手术后3周和30周后,分别通过Viewpoint视频系统对动物进行运动量检测,结果如图2所示,与对照动物相比,AAV-Exon1-103Q-GFP注射动物3周后总的运动距离缩短(Fig 2B),30周后,其中1只注射动物运动活性明显增加(Fig 2E)。 (2)取物试验(Object retrieval task) 在脑立体定位注射AAV-Exon1-103Q-GFP手术后,通过取物试验检测模型组和对照组动物的运动和认知功能水平。与对照组相比,注射组动物并未出现明显的认知障碍(Fig 2F-I)。
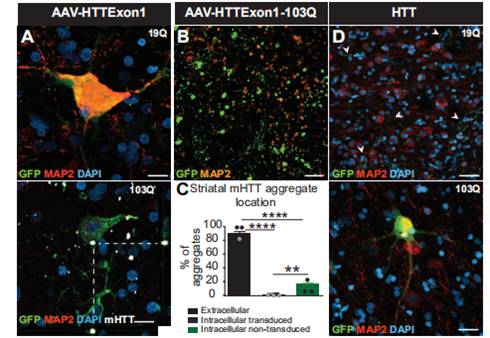
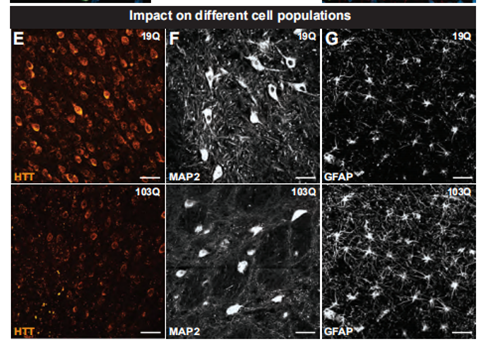
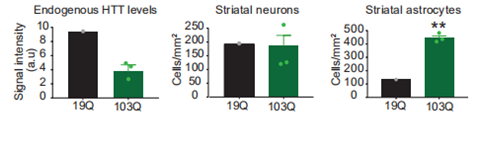
Fig 2. Behavioral changes in adult WT non-human primates receiving multiple bilateral striatal AAV2/6-HTTExon1-103Q injections. (A) Timeline of experiments and schematic showing location, volume of injections and number of animals used in each group. (B-E) Motor performance was evaluated by distance travelled in the open field at (B, C) 3 and (D, E) 30 weeks post-injection. (F-I) Cognitive behavior was assessed using the object retrieval test over a 6-week testing period. The object retrieval test was subdivided into (F-G) easy and (H-I) hard protocols. (3)病理学检测 绿色荧光信号(Fig 3A)显示转染成功。注射动物的纹状体细胞内和细胞外均有HTT蛋白的聚集(Fig 3B)。定量分析结果显示,大部分(82%)的HTT聚集物分布于神经元细胞外,而5.5%分布于神经细胞内,另外18.3%的神经细胞未转染病毒(Fig 3C)。这些HTT聚集物可播散至皮层(Fig 6D)。与对照相比,注射组恒河猴本身内源性的HTT水平降低(Fig 6E)。 对注射针剂周围神经元和胶质细胞的染色结果显示,mHTT并未明显减少神经元的数量(Fig 6F),但是星形胶质细胞出现明显的增生(Fig 6G)。
Fig 3. Reduction in endogenous primate HTT following striatal injection of AAV-HTTExon1-103Q-GFP injection. (A) Representative photomicrographs of AAV HTTExon1-19Q and -103Q in the striatum of injected primate brains. (B) Representative photomicrograph and (C) quantification of aggregate localization in the putamen of HTTExon1-103Q injected primates. (D) Low magnification photomicrographs of synaptically connected cortical regions of AAV HTTExon1-19Q and HTTExon1-103Q injected animals. (A-D) Neurons are labelled with MAP2 (red or orange), cell nuclei with DAPI (blue) and viral expression with GFP (green). (E) Representative confocal photomicrographs and quantification of endogenous HTT levels (red) in the cortex of injected primates. (F-G) Representative confocal photomicrographs and quantification of cell number for (F) MAP2 (red) and (G) GFAP (orange) in the putamen of AAV HTTExon1-19Q and -103Q injected primates. Data are expressed as mean +/- SEM. N = 1 19Q and N = 3 103Q. Scale bars: A: 10 µm; B, D-F: 20 µm. |
| 动物模型的评价与验证 |
我们以动物的一般表现和行为学改变来评价小鼠模型的症状表型。注射AAV-Exon1- 103Q-GFP30周后动物出现运动活性的增加。接近于临床的运动障碍表型。
我们从病理学进行模型的分析,结果显示注射动物的纹状体出现mHTT的聚集,这些HTT聚集物可播散至皮层。与对照相比,注射组恒河猴本身内源性的HTT水平降低。另外,mHTT聚集可引起星形胶质细胞明显的增生。与患者的病理表型相似。
目前没有确证有效的阳性药物。上市的丁苯那嗪和氘代丁苯那嗪,主要通过可逆性的抑制中枢神经系统的单胺转运蛋白2(VMAT2)来降低单胺类化合物,如5-羟色胺,多巴胺和去甲肾上腺素等的供应从而产生药理活性,并不适用于本模型。 |
| 保存方式 | 活体 |
| 合作方式 | 仅限合作研究 |
| 相关文章 | Use of adeno-associated virus-mediated delivery of mutant huntingtin to study the spreading capacity of the protein in mice and non-human primates. Neurobiol Dis. 2020;141:104951. |
| 备注 |


 京公网安备 11010502043083号
京公网安备 11010502043083号