| 标识符 | CSTR:16397.09.0C01001234 |
|---|---|
| 资源中文名称 | 新型冠状病毒(SARS-CoV-2)感染转基因小鼠模型 |
| 资源英文名称 | SARS-CoV-2 infected transgenic mice model |
| 疾病概述 | 新型冠状病毒肺炎起病以发热为主要的临床表现,可合并轻度干咳、乏力、呼吸不畅、腹泻等症状,流涕、咳痰等,咯痰症状少见。一半患者在一周后出现呼吸困难,严重者快速进展为急性呼吸窘迫综合征、脓毒症休克、难以纠正的代谢性酸中毒和出凝血功能障碍。部分患者起病症状轻微,可无发热等临床症状,多在1周后恢复。多数患者预后良好,少数患者病情危重,甚至死亡。从影像学表现来看,早期呈现多发小斑片影及间质改变,以肺外带明显。进而发展为双肺多发磨玻璃影、浸润影,严重者可出现肺实变,胸腔积液少见。从免疫学表现来看,患者还可出现发病早期外周血白细胞总数正常或减低、淋巴细胞计数减少,部分患者出现肝酶、肌酶和肌红蛋白增高。多数患者C反应蛋白和血沉升高,降钙素原正常。严重者D-D二聚体升高,淋巴细胞进行性减少。从组织病理学表现来看,患者表现为间质性肺炎,肺泡腔大量的多核巨细胞和巨噬细胞浸润,肺泡比弥漫性增厚,肺泡间隔增宽。 |
| 实验动物背景信息 | ICR |
| 模型制作方法 | SARS-CoV-2(原2019-nCoV, HB-01),由中国疾控中心谭文杰教授提供,通过滴鼻的方式感染人 hACE2 基因的小鼠,感染剂量1× 105 TCID50 只,感染体积50 μl 只。 |
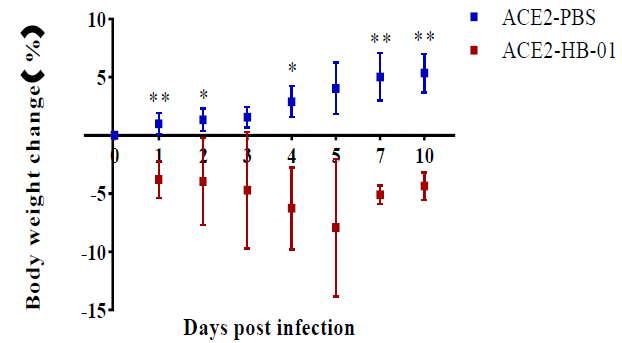
| 模型表型数据 | 3.1 临床表现 hACE2转基因小鼠感染后一般状态尚可,部分小鼠出现竖毛。感染后小鼠体重出现下降,感染 5天时平均体重下降百分比达到5%(图1)
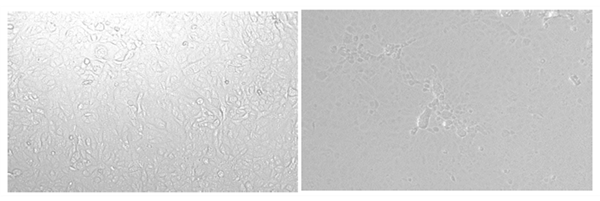
图1. hACE2 转基因小鼠感染后体重下降百分比. 与对照组相比, **p<0.01, *p<0.05. 3.2 病毒学检测 (1)病毒分离 感染第3天和第5天从肺组织分离病毒,匀浆接种Vero细胞,可发生有明显的细胞病变(图2),在电子显微镜下观察到病毒的特征性结构(图3)。而对照组小鼠没有观察到任何异常现象。
图2. Vero 细胞分离肺组织中病毒左侧:对照组小鼠;右侧: 感染组小鼠
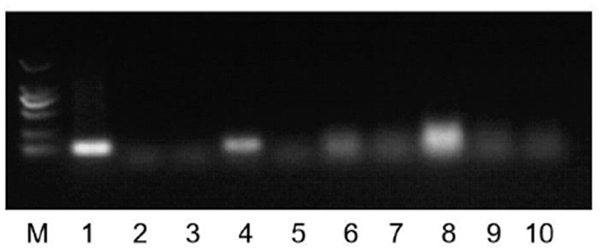
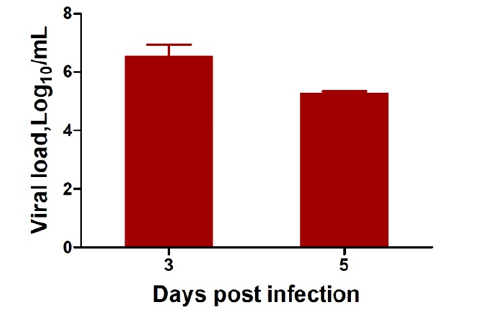
图3 电镜观察病毒结构 (2)病毒载量 在小鼠感染后第三天和第五天分别收集主要脏器,用以检测病毒在小鼠体内的分布情况。 RT PCR 结果显示,感染后 hACE2 转基因小鼠,只有在肺脏显现出病毒明显存在(图4)。 感染3 天后,肺组织中病毒载量可达到 106.5 拷贝/ml 感染 5 天后,肺组织中病毒载量可达到 10 5.0 拷贝/ml(图 5)。
图4 . RT-PCR检测肺组织中病毒核酸
图5 . RT PCR 检测肺组织中病毒(3 dpi 与5 dpi)
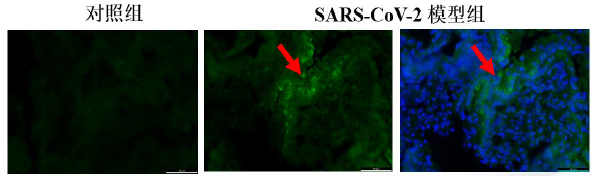
(3)病毒抗原检测 在小鼠感染后第三天和第五天分别收集主要脏器,用免疫荧光检查病毒在小鼠体内的分布情况,发现病毒主要分布于肺脏支气管上皮细胞和肺泡上皮细胞内 (图6)。
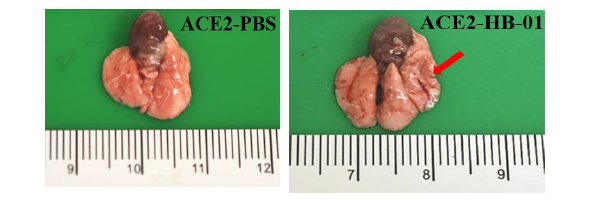
图6. 免疫荧光检查肺组织中病毒分部(3 dpi) 3.3病理学检查 (1)肺部大体病理 与对照组相比,感染小鼠肺脏大体病理表现为,肺脏表面出现局灶性病变损伤,呈暗红色。
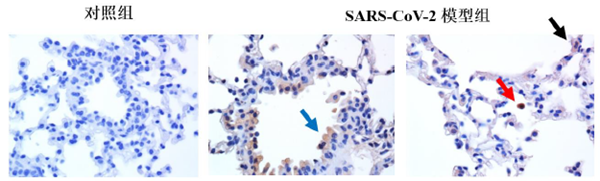
图7. 感染小鼠肺部大体病理. 左侧:对照组小鼠;右侧:感染组小鼠 (2)肺部组织病理 用免疫组化观察了肺组织内病毒抗原分布,发现抗原 分布于支气管上皮细胞(蓝箭头)、肺泡上皮细胞(黑箭头)和巨噬细胞(红箭头)(图8)。
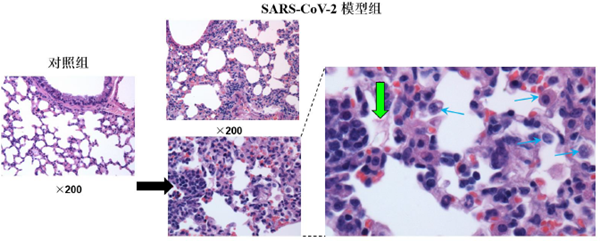
图8. 免疫组化观察肺组织内病毒抗原分布. 400 ×. 小鼠感染后肺组织呈弥漫性中度间质性肺炎改变,可见肺泡隔增宽、炎细胞浸润,血管周围炎细胞浸润(黑色箭头),肺泡腔内可见巨噬细胞(蓝色箭头)及少量蛋白(绿色箭头)渗出(图9)
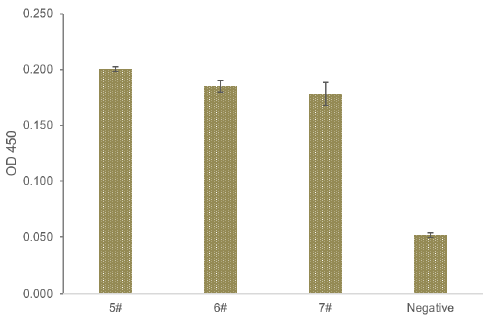
图9. 感染小鼠肺组织病理 3.3 抗体检测 感染小鼠第14天分离血清,检测到特异性IgG产生(图10)。
图10. 第 14天血清中抗体检测 |
| 动物模型的评价与验证 | 1. 动物模型评价方法 本实验建立的新型冠状病毒动物模型采用监测临床症状、病毒学和病理学 等方法进行分析和鉴定,确定该动物模型成功建立 。 (1)大体观察:临床症状观察包括动物的体重变化一般症状观察(弓背、竖毛、反应度降低等)等。动物感染后主要表现为明显的体重下降,部分动物竖毛,没有其他明显的症状。与其他传染病动物模型类似,体重下降百分比与疾病状态正相关。 (2) 病毒学监测发现,在肺组织中可以检测到病毒 RNA 并能分离到活病毒,在组织匀浆中电镜下可以观察到病毒颗粒,证实从被感染动物中可以分离到病毒,分别在感染后第3天和第5天检测到肺组织病毒载量,在病因上成功模拟 COVID 19。 (3)病理学检测发现,被感染动物的肺组织出现间质性肺炎呈弥漫性中度间质性肺炎改变,可见肺泡隔增宽、炎细胞浸润,血管周围炎细胞浸润,肺泡腔内可见巨噬细胞及少量蛋白渗出,在间质性肺炎和巨噬细胞浸润方面与临床一致。 以上三项指标模拟了新型冠状病毒感染肺炎病人的主要指标 ,证明小鼠模型成立。 2.评价指标体系 根据模型的主要表现,该模型用于研究、疫苗和药物评价时,与模型对照组相比,主要检测干预组的三类指标: (1)体重下降百分比 与模型对照组相比,观察感染小鼠的体重下降百分比改变情况。 (2)肺组织内病毒载量 与模型对照组相比,检测感染小鼠第3天和第5天肺组织内病毒载量变化情况。 (3)肺组织病理改变 与模型对照组相比,检测感染小鼠间质性肺炎的病理学改变情况。 |
| 保存方式 | 活体 |
| 合作方式 | 仅限合作研究 |
| 相关文章 |
[1]. Zhu, N., et al., A Novel Coronavirus from Patients with Pneumonia in China, 2019. New England Journal of Medicine, 2020. [2]. Wang, C., et al., A novel coronavirus outbreak of global health concern. The Lancet, 2020. [3]. Lu, R., et al., Genomic characterisation and epidemiology of 2019 novel coronavirus: impli cations for virus origins and receptor binding. The Lancet, 2020. [4]. Yang XH 1, et al., Mice transgenic for human angiotensin converting en zyme 2 provide a model for SARS coronavirus infection. Comp 2007 Oct;57(5):450 9. |
| 备注 |



 京公网安备 11010502043083号
京公网安备 11010502043083号